Thu hồi toàn quốc lô thuốc Alfachim 4.2 của Dược phẩm Cửu Long do không đạt chất lượng

TPO - Cục Quản lý Dược (Bộ Y tế) đã có thông báo thu hồi trên toàn quốc đối với lô thuốc viên nén Alfachim 4.2 do Công ty Cổ phần Dược phẩm Cửu Long sản xuất, sau khi lô thuốc này bị phát hiện không đạt tiêu chuẩn chất lượng.
Lô thuốc bị thu hồi có nhãn là Alfachim 4.2 (chứa Chymotrypsin tương đương 4200 IU), số lô 03010624, ngày sản xuất 1/06/2024, hạn dùng 1/06/2026, số đăng ký VD-34573-20.
Đây là loại thuốc có tác dụng chống phù nề và kháng viêm, thường được chỉ định trong các trường hợp phù nề sau chấn thương, bỏng hoặc hậu phẫu.
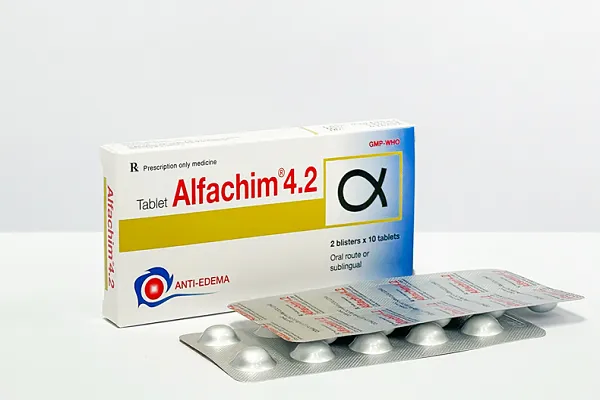 |
Lô thuốc viên nén Alfachim 4.2 bị yêu cầu thu hồi trên toàn quốc. |
Theo Cục Quản lý Dược, trước đó vào tháng 5/2025, Viện Kiểm nghiệm thuốc Trung ương đã tiến hành kiểm nghiệm mẫu thuốc Alfachim 4.2 và phát hiện mẫu không đạt tiêu chuẩn chất lượng về chỉ tiêu định lượng, vi phạm được phân loại ở mức độ 2.
Ngay sau khi có kết quả kiểm nghiệm, Cục đã yêu cầu thu hồi lô thuốc này tại Hà Nội và đề nghị Công ty Dược phẩm Cửu Long phối hợp lấy mẫu bổ sung, gửi kiểm nghiệm tại Viện Kiểm nghiệm thuốc Trung ương hoặc TP.HCM để xác minh chất lượng. Tuy nhiên, sau hơn 15 ngày theo yêu cầu, công ty không báo cáo kết quả kiểm nghiệm bổ sung mà chỉ nộp báo cáo về tình hình sản xuất, phân phối và thu hồi thuốc.
Sau đó, Công ty Cửu Long gửi văn bản đề nghị được thu hồi tự nguyện lô thuốc nói trên.
Trước tình hình này, Cục Quản lý Dược quyết định mở rộng thu hồi trên phạm vi toàn quốc, đồng thời yêu cầu Công ty Cửu Long phối hợp với các nhà phân phối khẩn trương thu hồi toàn bộ lô thuốc vi phạm và báo cáo kết quả thu hồi trước ngày 8/7/2025.
Cục cũng đề nghị các Sở Y tế tỉnh, thành phố và y tế các ngành thông báo đến các cơ sở kinh doanh, sử dụng thuốc về quyết định thu hồi; công bố thông tin thu hồi trên cổng thông tin điện tử; tổ chức kiểm tra, giám sát việc thực hiện và xử lý nghiêm các trường hợp không chấp hành theo quy định hiện hành.
Riêng Sở Y tế Hà Nội và Vĩnh Long, địa bàn có liên quan đến hoạt động sản xuất và phân phối thuốc của công ty được giao nhiệm vụ kiểm tra, giám sát toàn bộ quá trình thu hồi, đánh giá hiệu quả và xác định nguy cơ tiếp tục lưu hành thuốc vi phạm có thể gây ảnh hưởng xấu đến sức khỏe người dân.